Potencial de trabajo de la Energía
Trabajo= f( estado inicial, trayectoria de proceso, Estado final)
- Alrededores: todo lo que está fuera del sistema
- Alrededores Inmediatos: Corresponde a la porción de los alrededores que son afectados por el proceso.
- Ambiente: Región que se halla más allá de los alrededores inmediatos cuyas propiedades en cualquier punto que no son afectados por el proceso.
Estado Muerto:
Cuando el sistema se encuentra en equilibrio termodinámico con el ambiente, es
decir, que el sistema está a la temperatura y presión de su ambiente.
Trabajo Real (Nivel de Energía) > Trabajo Exergía
Siempre
hay una difrencia entre el trabajo real y la exergía
Exergía: Propiedad de la combinacion entre sistema y ambiente, y no del sistema
exclusivamente.
-
La Exergía de la energia cinetica Ec y de la energía potencial Ep, son
iguales a ellas mismas y estan completamenete disponible para trabajo.
-
La entalpía H y la energía interna U no
están disponibles para trabajo.
Un sistema entrega el máximo trabajo posible
cuando experimenta un proceso reversible del estado inicial especificado al
estado de su ambiente.
El Trabajo Reversible (Wrev): Cantidad máxima
de trabajo útil que puede producirse (o el trabajo mínimo que debe
suministrase)
Ejercicios
1) 8-16
Un
método de satisfacer la demanda adicional de potencia en los periodos pico es
bombear algo de agua de un gran cuerpo de agua (como un lago) a un depósito de
agua a mayor elevación en los tiempos de baja demanda y generar electricidad en
los tiempos de alta demanda dejando que esta agua baje y haga girar una turbina
(es decir, convertir la energía eléctrica en energía potencial y luego
nuevamente a energía eléctrica). Para una capacidad de almacenamiento de
energía de 5 x 106 kWh, determine la cantidad mínima de agua que se
necesita almacenar a una elevación promedio (relativa al nivel del suelo) de 75
m. Respuesta: 2.45*1010 kg
1)
8-17 ¿Qué
porción de la energía térmica de 100 kJ a 800 K se puede convertir a trabajo
útil? Suponga que el entorno está a 25 °C.
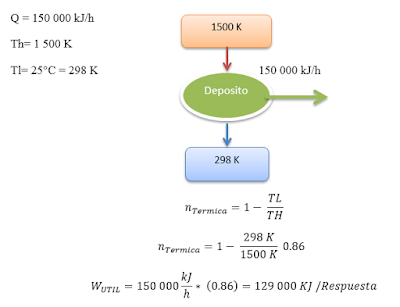
1) 8-19
Considere
un depósito de energía térmica a 1 500 K que puede suministrar calor a razón de
150 000 kJ/h. Determine la exergía de esta energía suministrada, suponiendo una
temperatura ambiente de 25 °C.
1)
Una máquina térmica recibe calor de una
fuente de 1200 K a una taza de 500 KJ/s y rechaza calor de desecho a un
ambiente a 300 K. La producción medida de potencia de la máquina térmica es de
180 kW. Determine a) la potencia reversible, b) la tasa de
irreversibilidad.
Nota: Los 195 KW se desperdician durante el proceso, la
diferencia de 500 KW y 375 KW es lo que
se puedes utilizar para el trabajo.
1) Un bloque de hierro de 500Kg, está inicialmente a
200°C y se deja enfriar a 27°C, transfiriendo calor hacia el aire a los
alrededores que se halla a 27°C. Determine el trabajo reversible y la
irreversibilidad para este proceso.
Nota: El calor especifico del hierro es de
0.45Kj/Kg K para este proceso. Considere que el sistema es cerrado y que la
energía cinética y potencial es despreciable. El proceso no involucra
interacciones de trabajo.
1)
8-18 Una máquina térmica que
recibe calor de un horno a 1 200 °C y rechaza calor de desecho a un río a 20 °C
tiene una eficiencia térmica de 40 por ciento. Determine la eficiencia de la
segunda ley de esta planta de potencia.
FUENTE:
CENGEL, YUNUS .A. & BOLES, MICHAEL A. (2011). Termodinámica. México: Mcgraw - Hill
















No hay comentarios:
Publicar un comentario